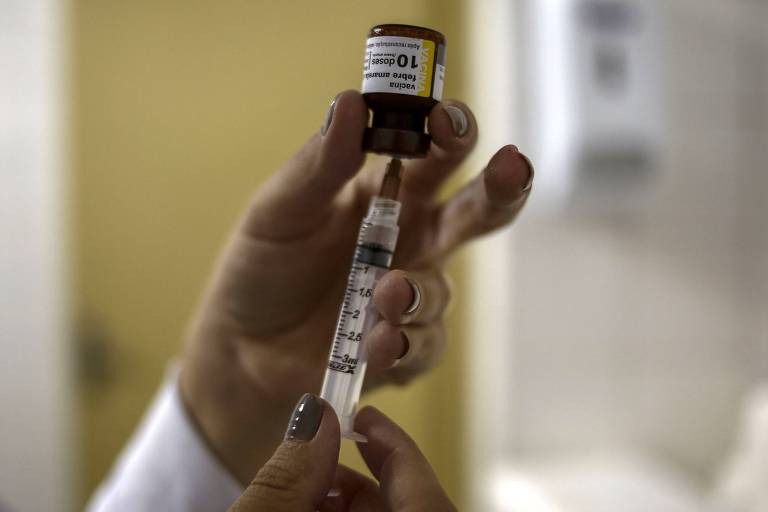
Diante do avanço dos casos de febre amarela no Brasil, o instituto que fornece as vacinas contra a doença ao Ministério da Saúde buscará antecipar sua produção e já interrompeu as exportações para outros países –para atender apenas a demanda nacional.
À frente da equipe que corre contra o relógio para que isso aconteça, Mauricio Zuma, diretor do Instituto de Tecnologia em Imunobiológicos Bio-Manguinhos, vinculado à Fiocruz, diz que a antecipação poderia ter efeitos em abril, ainda dentro do período com tradicionalmente maior circulação do vírus (que vai de janeiro a maio).
Ao todo, Bio-Manguinhos, maior fabricante mundial da imunização, deve produzir 48,3 milhões de doses neste ano –menos que em 2017, quando foram 60 milhões.
Mauricio Zuma, 58
Idade
58 anos
Formação
Doutor em gestão de tecnologia e inovação pela Universidade de Sussex e mestre em Gestão de Ciência e Tecnologia em Saúde pela Escola Nacional de Saúde Pública (Ensp/Fiocruz)
Cargo anterior
Diretor-executivo da Fundação para o Desenvolvimento Científico e Tecnológico em Saúde (2011 a 2017)
Aumentar o volume agora até seria possível, mas comprometeria a entrega de outras vacinas, como a tríplice viral (sarampo, caxumba e rubéola), segundo Zuma.
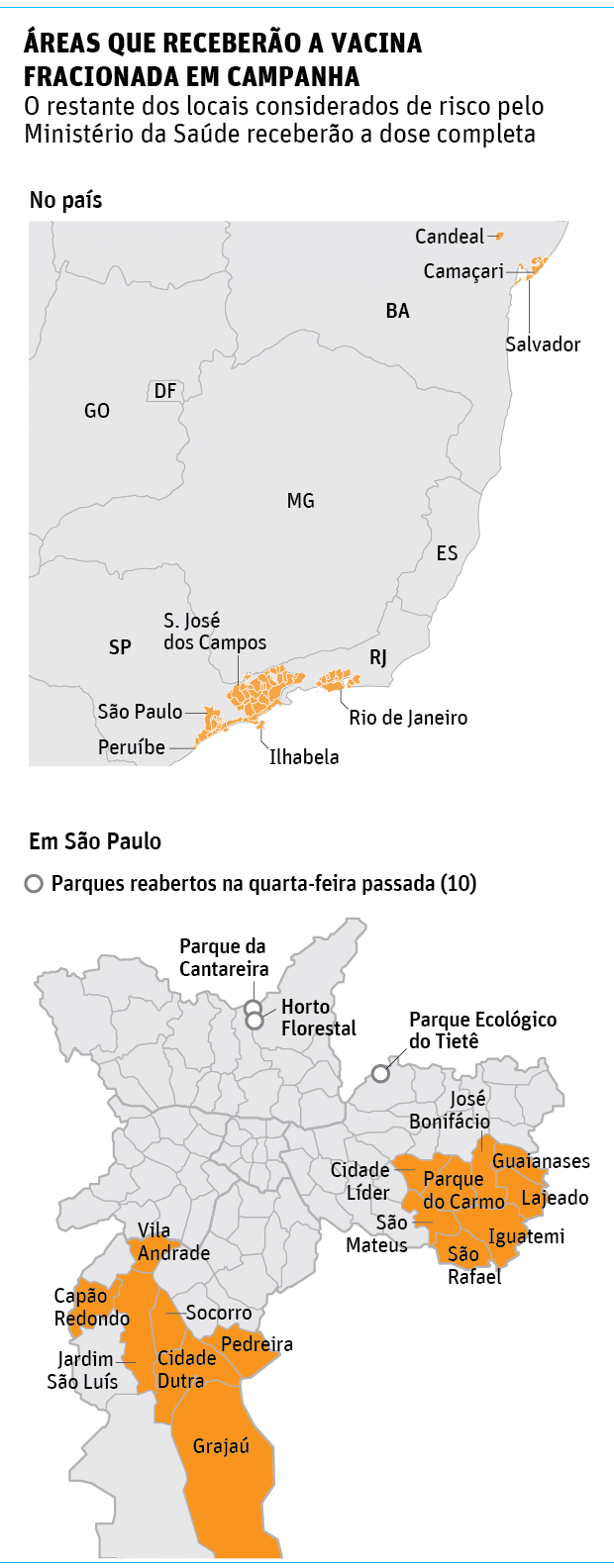
O avanço dos casos de febre amarela tem provocado longas filas pelo país, falta de vacinas em postos e levou a OMS (Organização Mundial da Saúde) a incluir o Estado de São Paulo inteiro no mapa de risco -com recomendação de vacinação para quem visitar a região.
Em entrevista à Folha, Zuma conta ainda que o instituto busca alternativas para fazer parte da produção fora, como parceria com um laboratório privado, e realiza pesquisas para novas formulações do produto, que causariam menos efeitos colaterais para grupos que, hoje, têm contraindicações à imunização.
Folha - Qual é a perspectiva de produção de vacinas em Bio-Manguinhos neste ano?
Mauricio Zuma - Fizemos um acordo no ano passado com o Ministério da Saúde para fornecer 48,3 milhões de doses. Agora, o PNI (Programa Nacional de Imunizações) está conversando conosco na perspectiva de tentar antecipar algumas das entregas que já estavam acordadas. Estamos trabalhando para antecipar parte da produção. Estamos estudando para quanto e para quando.
A produção é para o Brasil ou também para exportação?
Tem solicitação de fora, temos pedidos das Nações Unidas para exportar, mas a gente não se comprometeu ainda porque não sabemos se teremos capacidade. Se tiver capacidade de aumentar, seria para o Brasil –a não ser que o país não vá precisar [de mais vacinas] mais para frente, porque a gente sabe que, a partir de meados do ano, esses surtos vão diminuindo. No inverno, geralmente é menos problemática essa demanda por vacinas.
Existe a possibilidade de aumentar a produção?
Existe alguma possibilidade de aumentar a produção, mas a gente não consegue fazer isso muito rápido e, para isso, a gente tem que definir outras vacinas que o ministério precisa muito...
Como a tríplice viral?
Sim, tem vacina que concorre com a da febre amarela.
Quando as exportações foram suspensas?
Em meados do ano passado, a gente entregou 2,8 milhões de doses, porque já havia um compromisso para elas. Depois a gente suspendeu a exportação para atender a demanda do PNI.
É preciso lembrar que a nossa produção para 2017 para o ministério já estava acordada desde meados de 2016.
Naquele momento, não havia necessidade de um grande número de vacinas. Então, no final do ano, quando a situação começou a mudar, o PNI solicitou que a gente aumentasse a produção. Estamos conseguindo fornecer três vezes mais do que vínhamos fornecendo normalmente. Mas, para isso, tivemos que interromper qualquer possibilidade de importação para focar no Brasil, que é a nossa prioridade máxima.
Deve haver alguma mudança na produção de vacinas de febre amarela neste ano?
Neste ano, estamos adotando uma nova estratégia, que é contratar uma empresa farmacêutica brasileira [Libbs] que vai fazer uma parte da produção, o processamento final, para a gente. Esse processo hoje está sob análise para validação da Anvisa [Agência Nacional de Vigilância Sanitária] e deve ser aprovado até o final de maio, para que a gente consiga entregar produtos produzidos lá a partir de junho.
O avanço do vírus em direção ao Sudeste já vem acontecendo há algum tempo. Não teria sido possível aumentar a produção antes?
O volume de produção é monitorado e definido pelo PNI. Isso teve uma evolução inesperada, o vírus começou a circular de uma forma que não vinha circulando. Mas posso dizer que, da parte de Bio-Manguinhos, nunca faltou vacina. E da parte do PNI também nunca faltou disponibilidade para os Estados.
Eu acho que foi realmente um fator inesperado que está pegando todos de surpresa e que traz lições para todos.
Por exemplo?
Estamos antecipando alguns projetos. Temos um que deve estar registrado pela Anvisa ate o primeiro trimestre do ano que vem, que vai dobrar nossa capacidade de produção de concentrado viral, que é a primeira etapa de produção. Por ora, ainda estamos fazendo testes demorados, a Anvisa também leva algum tempo para analisar, mas teremos uma nova formulação para a vacina que vai nos permitir dobrar a capacidade do concentrado, que hoje é o maior gargalo.
O que muda exatamente?
Algumas das etapas do processo de produção desse item, principalmente a fase de formulação. Vamos poder usar menos embriões [a vacina é feita a partir de ovos embrionados de galinha] e estamos aproveitando para tornar a vacina mais pura através da retirada de alguns componentes. Só que isso requer estudos muito complexos, detalhados, documentados.
Há algum estudo para produzir vacina que não seja feita a partir do vírus atenuado?
Sim, temos projeto para produzir vacina com o vírus inativado. O desenvolvimento ainda está em um estágio inicial. Fazer uma vacina é algo que leva de cinco a dez anos. Só os estudos clínicos levam mais de cinco anos. A ideia é que ela possa ser usada por grupos que têm problema para usar a vacina atual. Por exemplo imunodeprimidos, gestantes, bebês. Seria uma vacina que talvez não tenha tanta efetividade quanto a nossa atual, mas seria bem adequada para alguns públicos por ser menos reatogênica [causar menos reações do organismo].
E temos um projeto revolucionário, uma plataforma vegetal, que pode demorar mais ainda.
Como seria?
É uma tecnologia muito nova. Hoje já trabalhamos com um biofármaco em que você expressa o antígeno [partícula que deflagra a produção de anticorpos] nas células de cenoura. Na vacina de febre amarela, a tentativa seria fazer o mesmo em folhas de tabaco. É uma tecnologia muito nova.
Qual é a maior dificuldade na produção da vacina? Faltou ou falta dinheiro?
Não faltou. A maior dificuldade é o grande quantitativo em curto espaço de tempo. Temos como produzir ao longo do tempo. Possivelmente daqui para frente o PNI queira formar um estoque estratégico maior. Mas o estoque é calculado de acordo com a realidade, senão você acaba jogando vacina fora. Tem que ser algo muito bem calculado para não desperdiçar recursos e não deixar a população desassistida. Agora, se você tem mudanças bruscas, acaba ficando difícil.



Comentários
Os comentários não representam a opinião do jornal; a responsabilidade é do autor da mensagem.