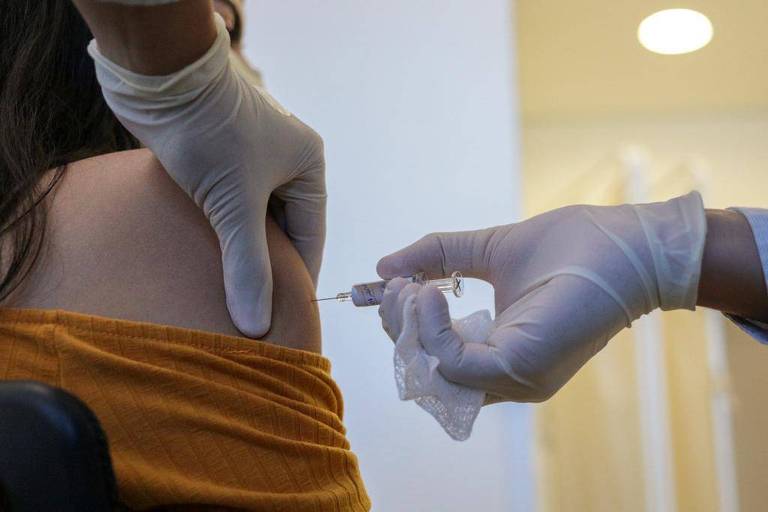
Anvisa (Agencia Nacional de Vigilancia Sanitaria) autorizó el miércoles (11) la reanudación de los ensayos de la vacuna Coronavac, producida por la empresa china Sinovac y el Instituto Butantan.
Las pruebas se suspendieron el lunes (9) después de que la agencia informara que había recibido una notificación de un evento adverso grave en un voluntario. Según la agencia, el objetivo era verificar los datos de seguridad y riesgo / beneficio.
Según el director del Instituto Butantan, Dimas Covas, la muerte del voluntario no tuvo relación con la vacuna. La hipótesis que barajan las autoridades es que el voluntario, un químico de 32 años, cometiese suicidio o haya sufrido una sobredosis. El informe policial, obtenido por Folha, registra el caso como "suicidio consumado".
Un parecer de un comité internacional independiente recibido por Anvisa el martes por la tarde (10) también descartó la relación con la vacuna.
A través de un comunicado, Anvisa informó el miércoles (11) que, "tras analizar los nuevos datos presentados por el patrocinador después de la suspensión del estudio, entiende que tiene suficientes subsidios para permitir la reanudación de la vacunación y sigue de cerca la investigación del caso [del voluntario] para que se descarte la posible relación causal entre el EAG inesperado y la vacuna".
Traducido por AZAHARA MARTÍN ORTEGA